- Heim
- Ressourcen
- Bloggen
- Edelstahl auf der Suche nach rostfreiem Stahl: Von der Elementzusammensetzung bis zu den Stahlsorten
Ein umfassendes Verständnis von Edelstahl: Vergangenheit, Gegenwart und Zukunft
Die Ursprünge und die Geschichte von Edelstahl: Eine Zeitleiste
- Im Jahr 1794: Der französische Chemiker Louis Nicolas Vauquelin untersuchte Krokoit-Erz (Bleichromat) und konnte erfolgreich Chromtrioxid (CrO3) herstellen, indem er das Erz mit Salzsäure vermischte. 1797 gelang es ihm, metallisches Chrom zu isolieren, indem er dieses Oxid in einem Holzkohleofen erhitzte. Vauquelin gilt damit als der wahre Entdecker des Elements Chrom.
- Im frühen 19. Jahrhundert: Die britischen Wissenschaftler James Stoddart, Michael Faraday und Robert Mallet beobachteten die Beständigkeit von Chrom-Eisen-Legierungen gegenüber Oxidationsmitteln.
- 1821: Pierre Berthier entdeckte die Korrosionsbeständigkeit von Chrom-Eisen-Legierungen gegenüber bestimmten Säuren und schlug deren Verwendung bei der Herstellung von Besteck vor.
- 1840er Jahre: Stahlhersteller im englischen Sheffield und Krupp in Deutschland produzierten beide Chromstahl. Letzterer verwendete ihn in den 1850er Jahren zur Herstellung von Kanonen.
- 1869: J. Baur von den Chrome Steel Works in Brooklyn produzierte als erster in den USA chromhaltigen Stahl für den Brückenbau und erhielt 1869 ein US-Patent für Chromstahl. Anschließend erkannten die britischen Wissenschaftler John T. Woods und John Clark die Bedeutung des Chromgehalts für die Korrosionsbeständigkeit von Chromlegierungen und stellten fest, dass der Chromgehalt im Bereich von 5-30% liegen sollte.
- Ende der 1890er Jahre: deutscher Chemiker Hans Goldschmidt entwickelte ein aluminothermisches (Thermit-)Verfahren zur Herstellung von kohlenstofffreiem Chrom.

- 1904–1911:Einige Forscher, insbesondere der Franzose Leon Guillet, stellten Legierungen her, die heute als rostfreier Stahl gelten.
- 1911: Philip Monnartz berichtete über den Zusammenhang zwischen Chromgehalt und Korrosionsbeständigkeit.
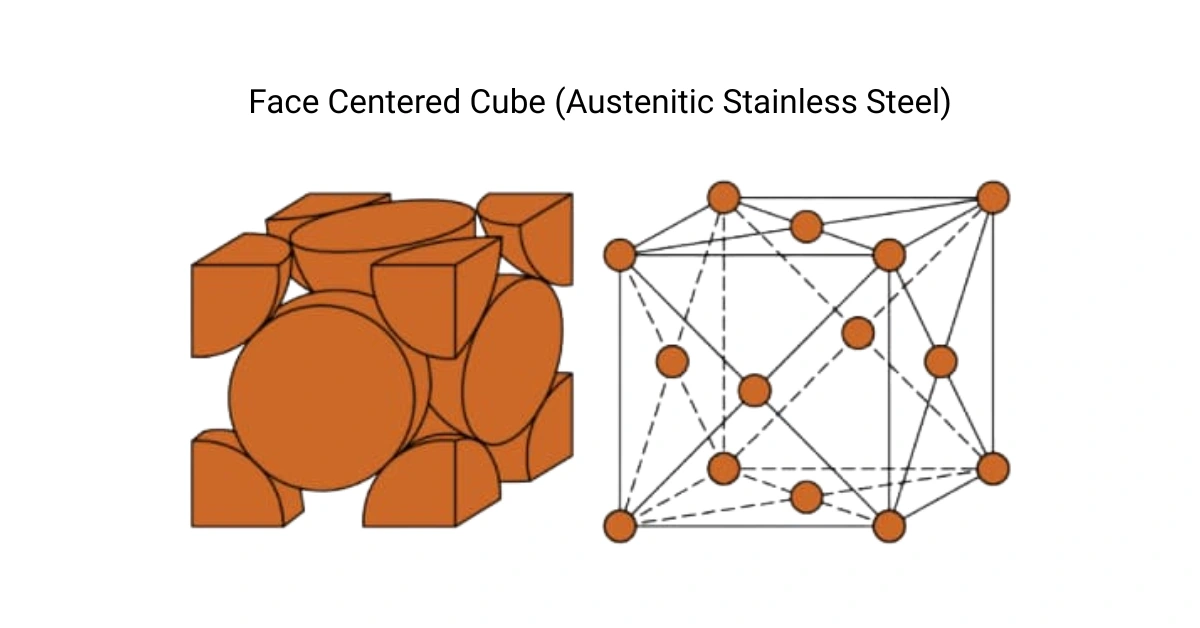
- 1912: Die Krupp-Ingenieure Benno Strauss und Eduard Maurer patentierten austenitischen Edelstahl (heute als 18/8 oder AISI Typ 304 bekannt).
- 1912: Auf der Suche nach einer korrosionsbeständigen Legierung für Gewehrläufe, Harry Brearley in Sheffield, England, entdeckte den heute als martensitischer Edelstahl Typ AISI 420 bekannten Stahl.

- 1915: Harry Brearleys Entdeckung wurde in der New York Times bekannt gegeben. Später arbeitete er mit Haynes zusammen und gründete mit einer Gruppe von Investoren die American Stainless Steel Corporation in Pittsburgh, Pennsylvania.
Elementare Zusammensetzung von Edelstahl: Der Schlüssel zur Rostvorbeugung
Edelstahl besteht hauptsächlich aus Eisen, Chrom, Nickel, Molybdän, Vanadium und anderen üblichen Legierungselementen. Eisen macht im Allgemeinen etwa 70 bis 80 Prozent des Edelstahls aus und sorgt für die notwendige strukturelle Festigkeit. Chrom ist für die Rostbeständigkeit von Edelstahl entscheidend. Damit Stahl als rostfrei gilt, sind mindestens 10,5 Prozent Chrom erforderlich, da dies für die Bildung einer stabilen, dichten Chromoxidschicht auf der Oberfläche unerlässlich ist. Diese Schicht ist sehr stabil und undurchlässig und verhindert wirksam das Eindringen von Sauerstoff und Feuchtigkeit bei Kontakt mit Luft oder Wasser, wodurch die Korrosionsbeständigkeit des Stahls deutlich verbessert wird.
Der Nickelgehalt liegt normalerweise zwischen 8% und 10%, was die Korrosionsbeständigkeit, Formbarkeit und Festigkeit von Edelstahl verbessert und dazu beiträgt, die nichtmagnetischen Eigenschaften von austenitischem Edelstahl bei niedrigen Temperaturen zu erhalten. Der typische Molybdängehalt liegt zwischen 2% und 3%, was die Beständigkeit gegen Lochfraß und Spaltkorrosion verbessert, was insbesondere unter chlorierten Bedingungen von Vorteil ist. Elemente wie Vanadium und Titan sind normalerweise in sehr geringen Mengen vorhanden und überschreiten normalerweise nicht 0,5%. Sie stärken Edelstahl, indem sie feine Carbide wie Vanadiumcarbid (VC) und Titancarbid (TiC) bilden, die die Struktur stabilisieren und Härte und Festigkeit verbessern. Diese Carbide sind aufgrund ihrer hohen Härte und Verschleißfestigkeit von entscheidender Bedeutung für die Verbesserung der Gesamtleistung von Edelstahl. Durch sorgfältige Anpassung der Anteile dieser Elemente kann Edelstahl in einer Vielzahl von rauen Umgebungen optimale Leistung erbringen.
Detaillierte Analyse des am häufigsten verwendeten Edelstahls 304: Zusammensetzung und Eigenschaften
Edelstahl 304 ist einer der vielseitigsten und am weitesten verbreiteten austenitischen Edelstähle, der für seine hervorragende Korrosionsbeständigkeit und Formbarkeit bekannt ist.
Zusammensetzung von 304 Edelstahl:
% | 304 | 304L | 304H |
C | 0,0 – 0,07 | 0,0 – 0,03 | 0,04 – 0,08 |
Mn | 0,0 – 2,0 | 0,0 – 2,00 | 0,0 – 2,0 |
Si | 0,0 – 1,00 | 0,0 – 1,00 | 0,0 – 1,0 |
P | 0,0 – 0,05 | 0,0 – 0,05 | 0,0 – 0,04 |
S | 0,0 – 0,03 | 0,0 – 0,02 | 0,0 – 0,02 |
Kr | 17.50 – 19.50 | 17.50 – 19.50 | 17.00 – 19.00 |
Ni | 8.00 – 10.50 | 8.00 – 10.50 | 8.00 – 11.00 |
Fe | Gleichgewicht | Gleichgewicht | Gleichgewicht |
N | 0.0-0.11 | 0.0-0.11 | 0,0 – 0,10 |
Eigenschaften von Edelstahl 304
| Klasse | 304 |
| Zugfestigkeit (MPa) | 500 – 700 |
| Dehngrenze (MPa) | 190 |
| Dehnung A50 mm | 45 Min. % |
| Härte Brinell | 215 Max HB |
| Eigentum | Wert |
| Dichte | 8,00 g/cm3 |
| Schmelzpunkt | 1450 °C |
| Elastizitätsmodul | 193 GPa |
| Elektrischer widerstand | 0,72 x 10-6 Ω.m |
| Wärmeleitfähigkeit | 16,2 W/mK |
| Wärmeausdehnung | 17,2 x 10-6/K |
Mikroskopische Perspektive: Der Rostschutzmechanismus von Edelstahl
Metallkorrosion bezeichnet Schäden, die durch die kombinierten Auswirkungen chemischer, physikalischer, mechanischer oder biologischer Faktoren in der Umgebung verursacht werden. Atmosphärische Korrosion, also die Verschlechterung von Metallmaterialien oder -strukturen aufgrund chemischer oder elektrochemischer Reaktionen unter atmosphärischen Bedingungen, ist die häufigste Korrosionsart. Weltweit werden über 60 % des Stahls unter atmosphärischen Bedingungen verwendet, darunter Stahlträger, Schienen, verschiedene mechanische Geräte und Fahrzeuge. Der Metallverlust durch atmosphärische Korrosion macht typischerweise mehr als 50 % des gesamten Korrosionsschadens aus.
Bei der normalen Metallkorrosion verliert Eisen Elektronen (oxidiert) und wird in Eisenionen umgewandelt, die dann mit Wasser reagieren und hydratisierte Eisenoxide (Rost) bilden.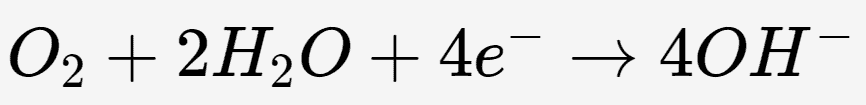
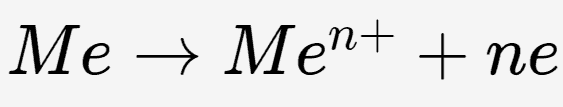
In Edelstahl, der einen hohen Chromanteil aufweist, reagiert das Chrom mit Sauerstoff in der Umgebung (Luft oder Wasser) und bildet eine dünne und stabile Chromoxidschicht auf der Metalloberfläche. Diese Chromoxidschicht ist unglaublich dünn und dennoch sehr haftend. Sie verhindert effektiv die für die Eisenoxidation notwendige Elektronenwanderung und isoliert das Eisen physisch von Oxidationsmitteln in der Umgebung.
Sollte die Oxidschicht vorübergehend mechanisch beschädigt oder chemisch zerstört werden, kann das Chrom im Edelstahl den Oxidfilm spontan regenerieren und die Oberfläche repassivieren. Diese selbstheilende Eigenschaft ist in Umgebungen von entscheidender Bedeutung, in denen das Metall häufig Verschleiß oder starker chemischer Belastung ausgesetzt ist.
Die Legierungszusammensetzung von Edelstahl enthält typischerweise Nickel und Molybdän, die die Stabilität der Oxidschicht verbessern, insbesondere in chloridhaltigen Umgebungen (wie Küstengebieten oder Tausalzbedingungen), und so das Risiko von Lochfraß und Spaltkorrosion verringern. Die Stabilität der Oxidschicht bleibt auch unter sauren oder stark oxidierenden Bedingungen erhalten, wodurch Edelstahl für eine Vielzahl von atmosphärischen Bedingungen geeignet ist.
Einschränkungen von Edelstahl: Wann korrodiert er?
- Chloride: Chloride können, insbesondere bei hohen Temperaturen, die Passivierungsschicht von Edelstahl beeinträchtigen und zu lokaler Korrosion und Lochfraß führen. Dies ist häufig in Meeresumgebungen und bei im Winter auf Straßen verwendeten Streusalzen zu beobachten.
- Starke Säuren: Während Edelstahl der Korrosion durch schwache Säuren standhält, können starke Säuren wie Schwefelsäure und Salzsäure schnell in die Passivierungsschicht eindringen und erhebliche Korrosion verursachen.
- Starke Oxidationsmittel: Starke Oxidationsmittel wie Peroxide und bestimmte Säuren (z. B. Salpetersäure) können den Korrosionsprozess in Edelstahl beschleunigen.
- Umgebungen mit niedrigem Sauerstoffgehalt: In Umgebungen mit unzureichender Sauerstoffversorgung, wie beispielsweise Erde und Schlamm, kann sich die Passivierungsschicht von Edelstahl nicht effektiv regenerieren, wodurch das Korrosionsrisiko steigt.
- Hochtemperaturbedingungen: Bei hohen Temperaturen kann die Passivierungsschicht von Edelstahl reißen oder instabil werden, was den Korrosionsprozess beschleunigt, insbesondere in Gegenwart korrosiver Substanzen.
- Mechanische Beanspruchung: Spannungsrisskorrosion kann auftreten, wenn Edelstahl gleichzeitig Zugspannungen und korrosiven Umgebungen ausgesetzt ist, insbesondere in Gegenwart von Chloriden.
- Mikrobielle Aktivität: In einigen Fällen können die Stoffwechselprozesse von Mikroorganismen (wie Bakterien) korrosive Substanzen produzieren. Dieses Phänomen, bekannt als mikrobiologisch induzierte Korrosion (MIC), kann zur Bildung von Biofilmen auf der Oberfläche von Edelstahl führen und so die Korrosion fördern.

Edelstahlnormen: Sortierung von Edelstahl
Weltweit gibt es mehrere gängige Güteklassen für Edelstahl, die von verschiedenen Standardisierungsorganisationen festgelegt wurden, um den Anforderungen verschiedener industrieller und kommerzieller Anwendungen gerecht zu werden.
- US-Normen (AISI/ASTM): AISI (Amerikanisches Eisen- und Stahlinstitut) und ASTM (American Society for Testing and Materials) sind gängige Edelstahlklassifizierungen, darunter die 300er-Serie (wie 304, 316), die 400er-Serie und weitere. Diese Standards werden in den Vereinigten Staaten und weltweit häufig verwendet.
- Europäische Normen (EN/ISO): DE (Europäische Norm) Normen werden vom Europäischen Komitee für Normung herausgegeben und decken verschiedene Aspekte von Edelstahl ab, wie z. B. 1.4301 für 304, 1.4401 für 316 usw. Darüber hinaus ISO (Internationale Organisation für Normung) veröffentlicht außerdem einflussreiche Normen für Edelstahl.
- Deutsche Normen (DIN): Deutsche Industrienormen (DIN) genießen international große Bekanntheit, insbesondere im Maschinenbau und in der Fertigung in Europa und Asien.
- Japanische Normen (JIS): JIS (Japanese Industrial Standards) erfreuen sich insbesondere in Asien großer Beliebtheit, vor allem in der Elektronik- und Automobilindustrie.
- Britische Standards (BS): Britische Normen (BS) werden von der British Standards Institution entwickelt. Obwohl ihre direkte globale Auswirkung möglicherweise nicht so groß ist wie die von ASTM oder EN, sind sie in Großbritannien und vielen Commonwealth-Ländern dennoch von erheblicher Bedeutung.
- Chinesische Normen (GB): Chinas nationale Normen (GB) werden häufig bei Produkten verwendet, die in China hergestellt und exportiert werden. Sie orientieren sich oft an internationalen Normen und verweisen auf diese.
Hier einige Vergleiche von Edelstahlsorten nach unterschiedlichen Normen:
| China (GB) | Russisch (GOST) | Amerikanisch (ASTM) | Deutsch (DIN) | ISO |
| 1Cr17Mn6Ni5N | – | 201 | X12CrMnNiN 17-7-5 | A-2 |
| 1Cr18Mn8Ni5N | 12KH17G9AH4 | 202 | X12CrMnNiN 18-9-5 | A-3 |
| 1Cr17Ni7 | – | 301 | – | 14 |
| 1Cr18Ni9 | 12KH18H9 | 302 | DIN17440-96 X12CrNi18-9 | 12 |
| Y1Cr18Ni9 | – | 303 | X12CrNiS18-9 | 17 |
| 0Cr18Ni9 | 08KH18H10 | 304 | X5CrNi18-10 | 11 |
| 00Cr19Ni11 | 03KH18H11 | 304L | X2CrNi19-11 | 10 |
| 1Cr18Ni12 | 12KH18H12T | 305 | X4CrNi18-12 | 13 |
| 0Cr17Ni12Mo2 | 08KH17H13M2T | 316 | X5CrNiMo17-12-2 | 20/20a |
| 0Cr18Ni12Mo2Ti | 08KH17H13M2T | 316Ti S31635 | X6CrNiMoTi17-12-2 | 21 |
| 00Cr17Ni14Mo2 | 03KH17H14M2 | 316L | X2CrNiMo18-14-3 | 19/19a |
| 0Cr19Ni13Mo3 | 08KH17H15M3T | 317 | X5CrNiMo17-13-3 | – |
| 1Cr18Ni9Ti | 12KH18H10T | 321 | X6CrNitI18-10 | 11 |
| 0Cr18Ni10Ti | 08KH18H10T | 321 | X6CrNiTi18-10 | 15 |
| 0Cr18Ni11Nb | 08KH18H12B | 347 | X6CrNiNb18-10 | 16 |
| 0Cr13Al | – | 405 | X6CrAl13 | 5 |
| 1Cr17 | 12KH17 | 430 | X6Cr17 | 8 |
| 1Cr12 | 403 | X6Cr13 | 3 | |
| 1Cr13 | 12KH13 | 410 | X12Cr13 | 3 |
| 0Cr13Ae | 405 | X6Cr13 | 1 | |
| 2Cr13 | 20KH13 | 420 | X20Cr13 | 4 |
| 3Cr13 | 30KH13 | 420 | X30Cr13 | 5 |
| 1Cr17Ni2 | 14KH17H2 | 431 | X17CrNi16-2 | 96 |
Prüfmethoden für Edelstahl
- Magnetische Prüfung: Die meisten rostfreien Stähle, insbesondere austenitische Typen wie 304 und 316, sind unter normalen Bedingungen nicht magnetisch. Ein Test mit einem Magneten, um zu sehen, ob das Material angezogen wird, kann vorläufig feststellen, ob es sich um austenitischen rostfreien Stahl handelt. Diese Methode ist einfach und schnell und eignet sich für eine schnelle Identifizierung vor Ort. Es ist jedoch zu beachten, dass Kaltbearbeitung bei einigen rostfreien Stählen eine leicht martensitische Struktur hervorrufen kann, die leichten Magnetismus verursacht.
- Reagenzientests: Dabei werden spezielle chemische Reagenzien verwendet, die mit Metallionen in Edelstahl reagieren, um Farbveränderungen zur Komponentenidentifizierung zu beobachten. Beispielsweise färben sich Eisenionentests blau, nickelspezifische Reagenzien reagieren von rosa nach rot und chromspezifische Reagenzien färben sich bei der Reaktion von gelb nach grün. Diese Methode ist kostengünstig, einfach zu handhaben und für schnelle Feldanwendungen geeignet.

- Spektrometerprüfung: Spektrometer analysieren die spezifischen Wellenlängen des von einem Material emittierten oder absorbierten Lichts, um dessen chemische Zusammensetzung genau zu bestimmen. Beispielsweise können mit dem tragbaren XRF-Analysator von Olympus zum Testen von Edelstahl Elemente wie Eisen, Chrom und Nickel genau identifiziert werden. Diese Technologie eignet sich für hochpräzise Anwendungen, die eine detaillierte Analyse der Zusammensetzung erfordern.

Es ist wichtig zu beachten, dass die oben genannten Testmethoden nur die Zusammensetzung der Metalloberfläche analysieren können. Bei dickeren oder massiven Edelstahlprodukten sind diese Methoden nicht in der Lage, die innere Zusammensetzung genau zu ermitteln. Daher besteht die beste Strategie, um den Kauf gefälschter Edelstahlmaterialien oder -produkte zu verhindern, darin, zuverlässige Lieferanten zu wählen, die Materialzertifikate vorlegen.
Vorteile und Herausforderungen von Edelstahl
Edelstahl ist für seine außergewöhnliche Korrosionsbeständigkeit, hohe Festigkeit und Ästhetik bekannt und eignet sich daher für eine Vielzahl von Anwendungen, von architektonischen Entwürfen bis hin zu Industrieanlagen. Darüber hinaus bietet er eine hervorragende Hitzebeständigkeit und ist 100% recycelbar, was gut mit nachhaltigen Praktiken vereinbar ist.
Trotz seiner Vorteile kann Edelstahl besonders bei Großprojekten unerschwinglich sein, und seine hohe Festigkeit erfordert oft spezielle Bearbeitungswerkzeuge und -techniken. Darüber hinaus kann seine schlechte Wärmeleitfähigkeit und Anfälligkeit für Spannungsrisskorrosion in bestimmten Umgebungen, wie z. B. solchen mit Chloriden, seinen Einsatz in bestimmten Anwendungen einschränken.
Wie verschiedene Elemente zu Edelstahl kombiniert werden

- Schmelzen und Legieren: Die Produktion von Edelstahl beginnt mit dem Schmelzprozess. Zu den Rohstoffen gehören typischerweise Stahl aus Erzschmelzen, der direkt für die Edelstahlproduktion verwendet wird, recycelter Edelstahl und Ferrolegierungen wie Ferronickel. Diese Materialien werden in einem Elektroofen erhitzt, bis sie bei hohen Temperaturen schmelzen. Dabei werden Legierungselemente wie Chrom und Nickel hinzugefügt, um sicherzustellen, dass der geschmolzene Stahl die angegebene chemische Zusammensetzung erreicht.
- Entfernen von überschüssigem Kohlenstoff: Ein Argon-Sauerstoff-Entkohlungsofen (AOD) wird typischerweise verwendet, um Sauerstoff unter normalem atmosphärischem Druck in den geschmolzenen Stahl einzublasen und gleichzeitig Inertgase (Ar, N2) einzuspritzen. Dieser Prozess verfeinert und entkohlt, indem er das Argon-Sauerstoff-Verhältnis anpasst und den CO-Partialdruck reduziert, wodurch der Kohlenstoffgehalt auf ein sehr niedriges Niveau gesenkt und die Oxidation von Chrom im Stahl verhindert wird.
- Besetzung: Nach dem Konditionieren und Rühren wird der geschmolzene Stahl in Formen gegossen, um zu Brammen oder Barren zu erstarren.
- Warm- und Kaltwalzen:
- Ausgehend von Brammen, die erwärmt und anschließend in Vor- und Fertigwalzwerken zu Bandstahl verarbeitet werden.
- Das heiße Stahlband wird in einer laminaren Strömung auf eine voreingestellte Temperatur abgekühlt und anschließend von einem Haspel aufgewickelt.
- Die abgekühlte Spule weist eine oxidierte Oberfläche auf, die durch Glühen und Beizen entfernt wird.
- Einige warmgewalzte Produkte werden direkt verwendet, während andere zu kaltgewalzten Produkten weiterverarbeitet werden.
- Beim Kaltwalzen werden warmgewalzte Produkte mit einer Dicke von 3,0–5,5 mm verwendet, die anschließend mittels Kaltwalzanlagen gewalzt werden.
- Nach dem Kaltwalzen wird der Edelstahl geglüht, um die durch das Walzen entstandene Kaltverfestigung zu beseitigen.
- Durch das Beizen wird die beim Glühen entstandene Oxidschicht entfernt und eine Passivierungsbehandlung durchgeführt, um die Korrosionsbeständigkeit der Stahlplatte zu verbessern.

Innovative Entwicklung von Edelstahllegierungen
Innovation bei Edelstahllegierungen durch Anpassung des Elementverhältnisses
Die Leistung von Edelstahllegierungen kann durch Anpassung der Elementverhältnisse in ihrer chemischen Zusammensetzung optimiert und verbessert werden. Durch Erhöhen oder Verringern des Gehalts wichtiger Elemente wie Chrom, Nickel, Molybdän und Titan können die mechanischen Eigenschaften, die Korrosionsbeständigkeit und die thermische Stabilität von Edelstahl erheblich verändert werden. So verbessert beispielsweise eine Erhöhung des Chromgehalts die Oxidations- und Korrosionsbeständigkeit; eine höhere Nickelzugabe verbessert die Schlagfestigkeit bei niedrigen Temperaturen und die allgemeine Zähigkeit; und für Anwendungen in Hochtemperaturumgebungen kann eine Erhöhung des Molybdängehalts erforderlich sein.
Diese Feinabstimmung der Elemente geht nicht nur auf spezielle industrielle Anforderungen ein, sondern führt auch zur Entwicklung neuer Edelstahlsorten für spezielle Anwendungen.
Beispiel: Edelstahl in Musks Raumschiff
SpaceX von Elon Musk hat für sein Starship-Projekt eine innovative Edelstahllegierung – 30X-Edelstahl – übernommen. SpaceX behauptet, dass 30X-Edelstahl ein neuer Typ von Edelstahl der 300er-Serie ist, der speziell für das Starship entwickelt wurde und im Vergleich zu herkömmlichem 304L-Edelstahl eine bessere Zähigkeit bei niedrigen Temperaturen bietet, während er bei hohen Temperaturen seine Festigkeit und Stabilität behält.

Die innovative Anwendung von SpaceX zeigt nicht nur das Potenzial der Anpassung chemischer Zusammensetzungen zur Optimierung der Edelstahleigenschaften, sondern unterstreicht auch die Bedeutung moderner Werkstoffe in der modernen Luft- und Raumfahrtindustrie. Durch solche Fortschritte werden bei der Entwicklung von Edelstahllegierungen die Grenzen industrieller Werkstoffe schrittweise erweitert und mehr Möglichkeiten für Anwendungen unter extremen Bedingungen geschaffen.
Fortschrittliche Fertigungstechnologien: Die Zukunft von Edelstahl
Hocheffiziente und energiesparende Schmelzverfahren:
Bei der modernen Edelstahlproduktion kommen Lichtbogenöfen (EAF) und Induktionsöfen mit modernen Steuerungssystemen zum Einsatz. Diese Technologien verbessern die Präzision des Schmelzens, die Reinheit der Materialien und reduzieren Energieverbrauch und Umweltbelastung.
Fortschritte bei Raffinations- und Verunreinigungsentfernungstechniken:
Mithilfe der Technologien Argon-Sauerstoff-Entkohlung (AOD) und Vakuum-Sauerstoff-Entkohlung (VOD) lassen sich Verunreinigungen wirksam aus Edelstahl entfernen, seine chemische Zusammensetzung optimieren und seine mechanischen Eigenschaften und Korrosionsbeständigkeit verbessern.
Präzise Kontrolle mikrostruktureller Phasen:
Durch Steuerung der Abkühlraten und Glühtemperaturen während der Wärmebehandlung kann das Verhältnis von Austenit zu Ferrit angepasst werden, um optimale mechanische Eigenschaften und Korrosionsbeständigkeit zu erzielen.
Stranggusstechnik:
Durch Strangguss wird die Produktion von Edelstahl durch Automatisierung des Gießens von flüssigem Stahl in Knüppel und Brammen revolutioniert. Diese Methode verbessert die Ausbeute, senkt den Energieverbrauch und gewährleistet Produktkonsistenz, wodurch die mit dem traditionellen Barrenguss verbundenen Defekte minimiert werden.
Laser-3D-Druck und andere additive Fertigungstechnologien:
Additive Fertigung, darunter selektives Laserschmelzen (SLM) und Elektronenstrahlschmelzen (EBM), ermöglicht die Herstellung komplexer Edelstahlkomponenten mit maßgeschneiderten Eigenschaften.

In diesen Abschnitten werden die innovativen Techniken und Technologien beschrieben, die die Zukunft der Edelstahlproduktion prägen, wobei der Schwerpunkt auf Nachhaltigkeit, Effizienz und fortschrittlichen Materialeigenschaften liegt.
Fazit
Die Verwendung von Edelstahl hat die industrielle Effizienz deutlich gesteigert und die Lebensdauer von Produkten verlängert, was sich auch positiv auf die Umwelt auswirkt. Aufgrund seiner Recyclingfähigkeit trägt Edelstahl dazu bei, Industrieabfälle und den Bedarf an Rohstoffen zu reduzieren und unterstützt so nachhaltige Industriepraktiken.
Darüber hinaus steigert Edelstahl die Lebensqualität erheblich. Seine weitverbreitete Verwendung von medizinischen Instrumenten bis hin zu Küchengeräten hat das tägliche Leben gesünder und bequemer gemacht. Darüber hinaus hat seine Verwendung in öffentlichen Sicherheitsstrukturen wie Transportfahrzeugen und -einrichtungen die öffentliche Sicherheit verbessert.
Zusammenfassend lässt sich sagen, dass Edelstahl nicht nur eine grundlegende Säule der modernen Industrie ist, sondern auch ein wichtiges Material, das die globale Gesellschaft zu mehr Effizienz und Nachhaltigkeit führt. Mit der kontinuierlichen Entwicklung neuer Technologien werden die Anwendungen und der Einfluss von Edelstahl voraussichtlich weiter zunehmen.
Entdecken Sie mehr mit unseren Blogbeiträgen.
kürzliche Posts
Erfahren Sie mehr über unsere Produkte
HDC-Produkte
Sofortiges Angebot!